未知タンパク質の同定、発現プロファイリング、新薬の開発や病気のメカニズムの解明、新規バイオマーカーの発見など、プロテオーム解析はさまざまな分野で活用されています。
このプロテオーム解析に強力な力を発するツールが質量分析です。MALDI-ToF MSやLC-MSなどがよく使用されており、現在は、液体クロマトグラフと質量分析計を組み合わせたLC-MSが主流です。より高精度に、より高感度にと歩を進めてきたLC-MS技術ですが、その中で、重要にも関わらず、面倒に思われることの多いステップがあります。
それは、サンプル調製ステップです。

これは、LC-MSのサンプルの調製には「標準的な方法」がないためです。サンプルタイプや実験目的によって、最適なプロトコルは異なります。また、タンパク質の抽出効率や再現性は高くなければなりませんし、LC-MSにかける前のペプチドサンプルの純度や質も高いものが求められます。そのため、LC-MSのサンプル調製の一般的な流れをベースにして、各ステップを最適化していく必要があります。
では、どのような点を気にして最適化すればよいのでしょうか。本ブログでは、LC-MSのサンプル調製のポイントについて、ご紹介します。
▼もくじ [非表示]
サンプル調製の流れ

図1. LC-MSの一般的なサンプル調製の流れ
図1にLC-MSで一般的に実施されているサンプル調製の流れを示しました。それぞれのステップのポイントをご紹介していきましょう。
タンパク質抽出
プロテオーム解析とは、「生体内のタンパク質の網羅的な解析」です。そのため、タンパク質抽出ステップでは、細胞や組織から、できる限り多くのタンパク質が抽出できる条件を選ぶ必要があります。同じ細胞や組織からMS解析を行った文献が参考になります。
ここで注意点があります。細胞や組織から多くのタンパク質を抽出するのに避けて通れないのが、界面活性剤(詳しくはこちら)です。しかしこの界面活性剤、一般的に、LC-MSに持ち込むことができません。ペプチドのイオン化を阻害したり、分析時のピークとして出てしまったり、カラムや流路に残り汚染の原因になるなど、解析に影響を与えるためです。さらに、界面活性剤の種類や濃度によっては、LC-MS前のトリプシンやLys-Cなどの酵素活性を阻害することもあります※1。
さらに、界面活性剤だけでなく、同じく抽出に使われることのある変性剤も、同様に酵素活性やLC-MSへの影響があります※1。
※1 参考情報
・トリプシン(Thermo Scientific™ Pierce™ Trypsin Protease, MS Grade):0.1% SDS、1M Urea、10% acetonitrile (ACN) 存在下で使用可能です。高濃度の塩(100mM以上のNaClなど)は活性に影響する場合があります。
・Lys-C(Thermo Scientific™ Pierce™ Lys-C Protease, MS Grade):0.1% SDS、8M Urea、10% acetonitrile (ACN) 存在下で使用可能です。
そのため、これらは、酵素消化の前までに除去するか、希釈をしておかねばなりません。除去方法についても注意が必要です。低分子の除去によく使われる透析は、一部の界面活性剤では使用できません(詳しくはこちら)。また、クリーンアップによく使われるC18などの逆相カラムでも界面活性剤の除去ができません。よって、界面活性剤の除去には、界面活性剤除去カラムやTCAアセトン沈殿などの手法を選びましょう。
タンパク質濃度測定
この後に続く還元・アルキル化・消化ステップではタンパク質量の目安が必要になります。また、選んだ抽出方法でどのくらいのタンパク質が抽出されたか確認をするためにも、ここでタンパク質の濃度測定をしておきましょう。
タンパク質濃度測定には、比色法がよく使われますが、どの比色法がよいかは、抽出試薬の組成によって異なります。抽出試薬の組成と濃度測定キットの適合性判断についてはこちらのブログをご参照ください。
還元・アルキル化
還元剤によりタンパク質のジスルフィド結合を切断し、かつ還元されたシステイン残基を不可逆的にアルキル化することで、消化酵素の効率や質量分析における配列カバー率を向上させることができます。
還元剤にはたいていDTTが使用され、また、アルキル化剤として最も広く使われている試薬はIAA(ヨードアセトアミド)です。
界面活性剤の除去など
サンプル抽出に界面活性剤を用いて除去が必要な場合、ここに除去ステップを追加することをおすすめします。界面活性剤は濃度や種類によって酵素消化に影響を及ぼすことがあり、また、図2のように、質量分析結果に影響を及ぼすためです。
界面活性剤は、上述のとおり、透析で除去できるものとできないものがあります。また、抽出試薬によっては、組成が開示されていないこともあり、どういった界面活性剤が含まれているのかが不明なこともあります。そういったときは、イオン性、非イオン性、両性イオン性の界面活性剤を除去できるカラムの使用や、TCAアセトン沈殿などが利用されます。
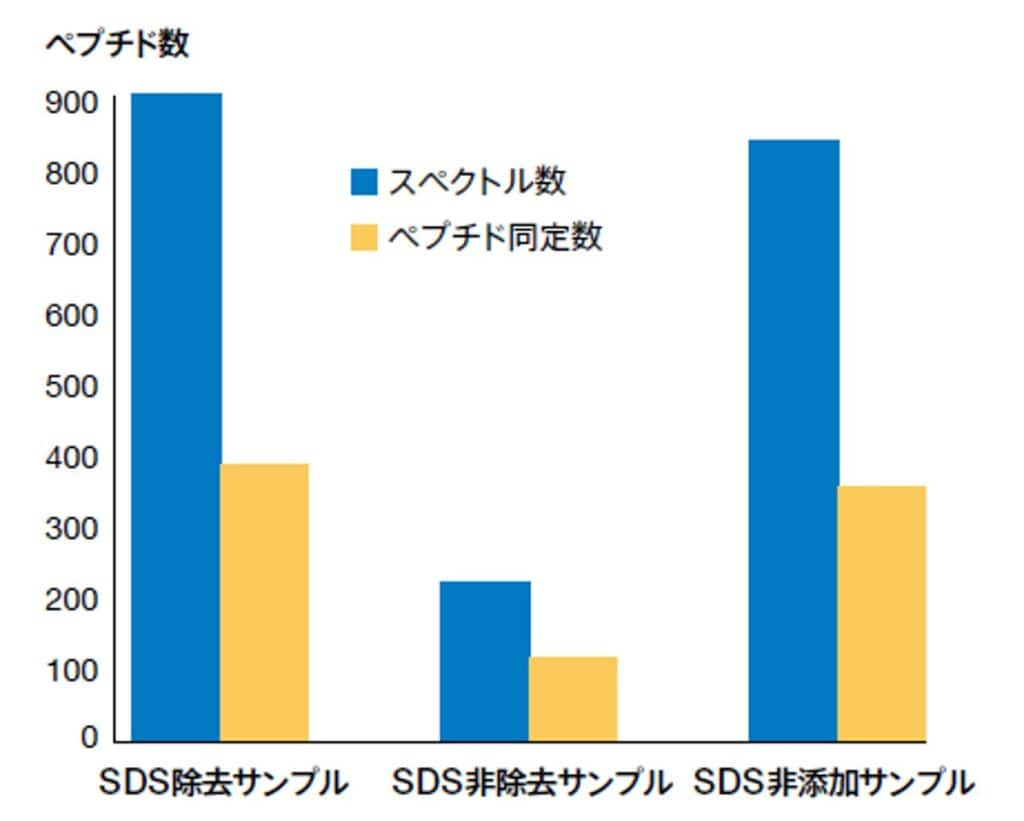
図2. SDS除去または非除去サンプルのスペクトル数とペプチド同定数の比較
1% SDSを含むHeLa細胞ライセートのトリプシン消化サンプル(0.1 mL, 100 μg)をThermo Scientific™ Pierce™ Detergent Removal Resin, 0.5 mLで処理した後、LC-MS/MSを行いました。SDSを除去したサンプルのペプチド同定数は、SDSを添加しない場合に近く、SDSを除去しない場合に比べて向上しています
酵素消化
質量分析における酵素消化では、消化効率や特異性が高いトリプシンがよく使われます。トリプシンは、リジン(K)やアルギニン(R)のC末端側のペプチド結合を切断します。これにより、質量分析において適当なサイズのペプチドを得ることができます。消化は、4~24時間で実施されることが多いです。
なお、トリプシンのK/R切断だけでは分析が困難な領域や、配列によっては十分に消化されないタンパク質があります。そういったケースではLys-Cとトリプシンの両方を用いたり(Thermo Scientific™ Trypsin/Lys-C Protease Mix)、異なる切断特異性を持つ酵素を用いたりすることで、質量分析におけるカバレッジを上げることができます。
クリーンアップ
クリーンアップで一般的によく使われるのは、C18などの逆相カラムです。クリーンアップの目的は、主に塩類やバッファーの除去です。これらの成分が残ったままだと、LC-MSの分析に影響を与えてしまうためです。なお、C18などの逆相カラムでは界面活性剤が除去できないことにご注意ください。
最後に、これら全てのステップにおいて、ケラチンの混入を防ぐために手袋をしての作業をおすすめします。
このように、LC-MS前のサンプル調製は、ステップごとに質量分析に影響を与えるか否か、与えるのであればその物質をどのように除去すればよいかを考えながら進める必要があります。しかし、ステップ数が増えると時間もかかりますし、煩雑性も増します。さらに、サンプルの量や質にバラつきが生じやすくなり、そして品質や再現性の低下は質量分析で得られる結果にも影響を及ぼします。
そのため、サンプル調製ステップの手間や時間を何とか最小限にし、かつ再現性を高めるために、各メーカーからいくつかキットが販売されています。Thermo Scientific™ EasyPep™ MS Sample Prep Kitsシリーズも、そのひとつです。
EasyPepで悩まずサンプル調製
EasyPepシリーズは、LC-MS前のサンプル調製の所要時間を節約しながら再現性が向上できるように設計されている製品です。
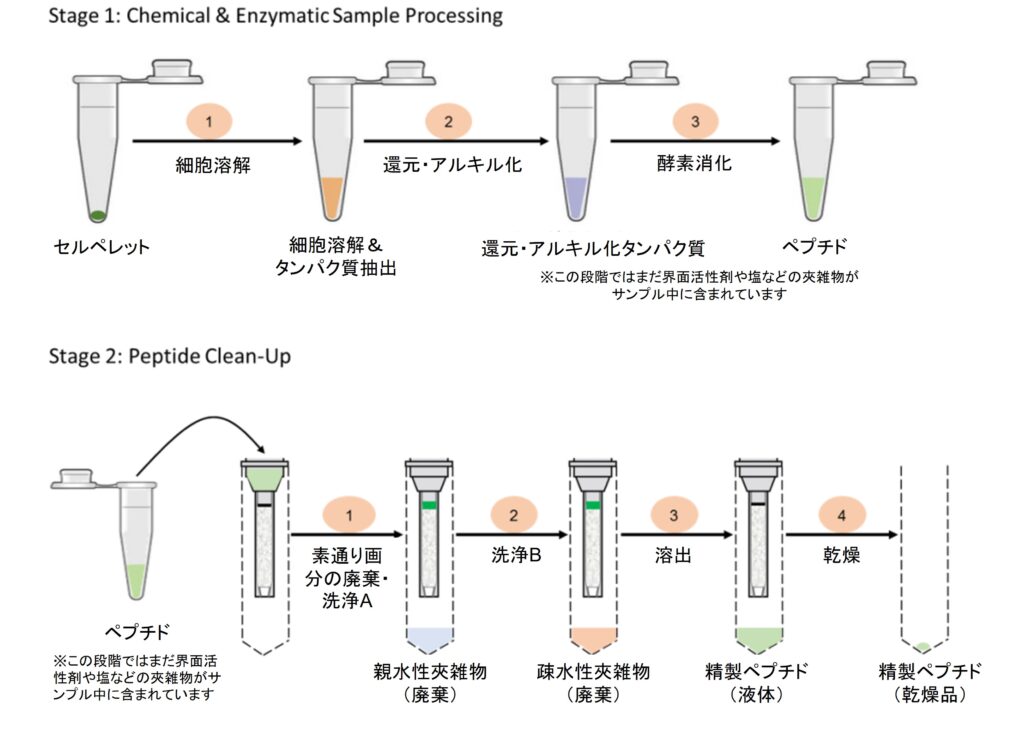
図3. EasyPepシリーズ使用の流れ※2
※2 製品によって詳細なプロトコルは異なりますので、必ずそれぞれの製品のユーザーガイドをご確認ください。
EasyPepシリーズのLysis Buffer(サンプル溶解用バッファー)は、組織・細胞などのサンプルにおいて高い抽出効率が得られやすく、かつ汎用性が高い組成にデザインされています。また、Lysis Buffer内には界面活性剤が含まれていますが、酵素消化には影響しない濃度で、かつ図2のクリーンアップ工程の中で除かれます。そのため、従来法のように除去工程を経る必要がありません。さらに、サンプル調製時に核酸の抽出により粘性が高くなった場合、従来法では超音波処理を行うことがありますが、EasyPepシリーズはUniversal Nucleaseが含まれているため、粘度低減のために超音波処理をする必要もありません。
以上はEasyPepシリーズの利点のほんの一部です。これら以外にも、EasyPepシリーズではすべてのステップが簡便かつ短時間で実施できるようデザインされているため、全工程が2~4時間で終了します(従来法では~2日)。何より、キット化されていますので、試薬をひとつずつ購入する必要がなく、また、界面活性剤や塩の除去の必要性や除去の方法に悩む必要がありません。
従来法と比べたEasyPepシリーズの主なメリットを下記にまとめました。
- 組織※3・細胞などのサンプルに対応
- タンパク質抽出から還元・アルキル化・酵素消化・精製まで必要な試薬すべてがキット化
- 別途、界面活性剤などの除去ステップを設ける必要なし
- 全工程が短時間(2~4時間)で完了
- 酵素はTrypsin/Lys-Cを使用し、カバレッジを向上
- クリーンアップは親水性・疎水性の夾雑物を両方除去
- TMTラベルにも対応
※3 オプションで、抽出時にホモジナイザーによる破砕を行います。
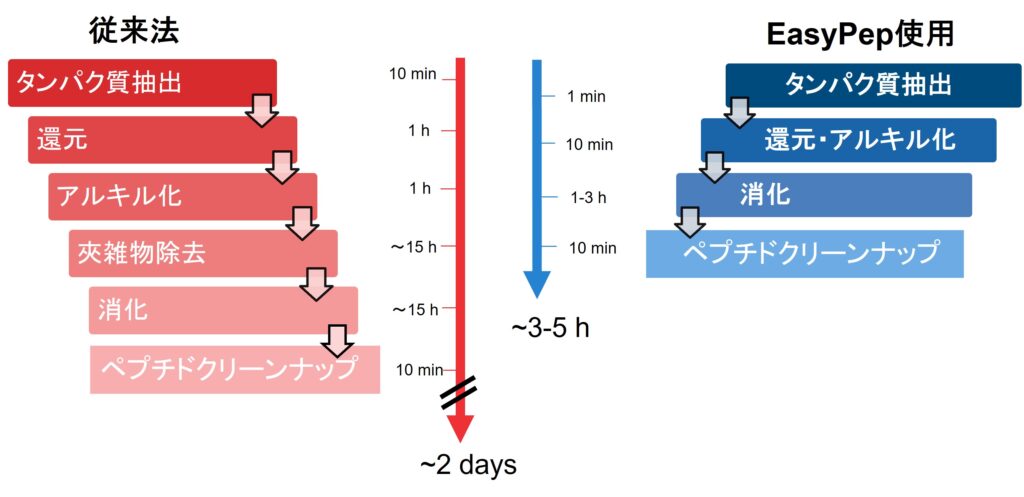
図4. 従来法とEasyPepTMシリーズ使用時の所要時間の違い
また、従来法とEasyPepシリーズでの調製を比べた結果、タンパク質同定数、ペプチド同定数ともに従来法と同等以上の結果が得られています。
EasyPepシリーズは、発売以降、非常に好評をいただいているキットで、論文での実績も日々増え続けています。これから質量分析を始める人にもおすすめですので、ぜひ使用を試してみてください。
まとめ
LC-MSのサンプル調製は、プロテオーム解析を成功させるために重要なステップのひとつです。しかし、決められたプロトコルがなく、ペプチドサンプルの純度や再現性を高くするために検討も必要で、煩雑性が高い複雑なステップです。EasyPepシリーズは、そんな研究者の負担や時間を軽減してくれる強力な味方です。有効に活用してみてください。
プロテオーム解析に最適なThermo Scientific™ Orbitrap™質量分析計はこちら
プロテオミクス基礎シリーズe-learningはこちら
質量分析前処理ハンドブック~プロテオーム解析に必須な試薬やツール
このブログを読んだ人はこんなブログも読んでいます:
界面活性剤を用いたタンパク質抽出|知っておきたい!タンパク質実験あれこれ 第1回
BCA法、Bradford法、Lowry法など、“総”タンパク質定量法の原理まとめ
研究用にのみ使用できます。診断用には使用いただけません。